| Inicio |
Equilibrio Térmico
|
Cambios de Estado
|
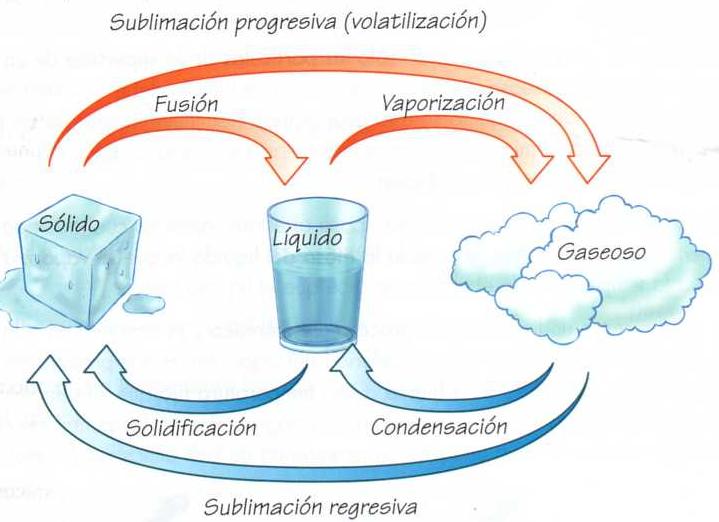
Cambios de estado
Cuando
un cuerpo, por acción del calor o del frío pasa de un estado a otro, decimos
que ha cambiado de estado. En el caso del agua: cuando hace calor, el hielo se
derrite y si calentamos agua líquida vemos que se evapora. El resto de las
sustancias también puede cambiar de estado si se modifican las condiciones en
que se encuentran. Además de la temperatura, también la presión influye en el
estado en que se encuentran las sustancias.
Los cambios de
estado están divididos generalmente en dos tipos: progresivos y regresivos.
Cambios progresivos:
Vaporización, fusión y sublimación
progresiva.
Cambios regresivos:
Condensación, solidificación y sublimación regresiva
Fusión
 Es
el paso de un sólido al estado líquido por medio
del calor; durante este proceso endotérmico (proceso que absorbe energía
para llevarse a cabo este cambio) hay un punto en que
la temperatura permanece constante. El "punto de fusión" es
la temperatura a la cual el sólido se funde, por lo que su valor es particular
para cada sustancia. Dichas moléculas se moverán en una forma
independiente, transformándose en un líquido. Un ejemplo podría ser un hielo
derritiéndose, pues pasa de estado sólido al líquido.
Es
el paso de un sólido al estado líquido por medio
del calor; durante este proceso endotérmico (proceso que absorbe energía
para llevarse a cabo este cambio) hay un punto en que
la temperatura permanece constante. El "punto de fusión" es
la temperatura a la cual el sólido se funde, por lo que su valor es particular
para cada sustancia. Dichas moléculas se moverán en una forma
independiente, transformándose en un líquido. Un ejemplo podría ser un hielo
derritiéndose, pues pasa de estado sólido al líquido.
Solidificación
Es el paso de
un líquido a sólido por medio del enfriamiento; el proceso
es exotérmico. El "punto de solidificación" o de congelación es
la temperatura a la cual el líquido se solidifica y permanece constante durante
el cambio, y coincide con el punto de fusión si se realiza de forma lenta
(reversible); su valor es también específico
Vaporización y ebullición
Son los procesos físicos en los
que un líquido pasa a estado gaseoso. Si se realiza cuando la
temperatura de la totalidad del líquido iguala al punto de
ebullición del líquido a esa presión continuar calentándose el líquido,
éste absorbe el calor, pero sin aumentar la temperatura: el calor se emplea en
la conversión del agua en estado líquido en agua en estado gaseoso, hasta que
la totalidad de la masa pasa al estado gaseoso. En ese momento es posible
aumentar la temperatura
del gas.
 |
El punto de
ebullición es
aquella temperatura en la cual la materia cambia de estado líquido a gaseoso,
es decir se evapora.
|
Condensación
Se
denomina condensación al cambio de estado de la materia que se pasa
de forma gaseosa a forma líquida. Es el proceso inverso a la vaporización.
Si se produce un paso de estado gaseoso a estado sólido de manera directa, el
proceso es llamado sublimación inversa. Si se produce un paso del estado
líquido a sólido se denomina solidificación.
Desionización: Es el cambio de un plasma a gas.
Ionización: Es el cambio de un gas a un plasma.
Centro de Bachillerato Industrial y de Servicios No. 37 Modulo de Física II
Profesor: Salvador Acosta Bordas Grupo: 5AMP
Investigación por:
Profesor: Salvador Acosta Bordas Grupo: 5AMP
Investigación por:
- Lopez Velasquez Luis Fernando
- Melendrez Rosas Jorge Antonio
- Ochoa Torres Carlos
- Pablos Hernandez Ddaayaanne
- Renteria Gerardo Ilse Madhelí